
《中国新药与临床杂志》

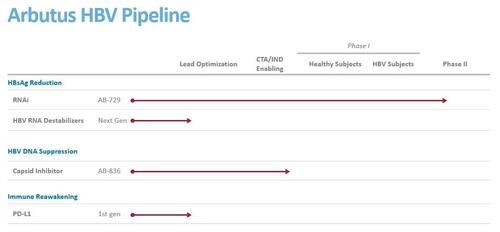
乙肝研究药企杨梅生物制药公司(Arbutus Biopharma Corporation),目前正在推进旗下2种乙肝在研新药,AB-729和AB-836。乙肝是一种由乙肝病毒引起的可能危及生命的肝脏感染疾病。Arbutus公司正在开发多种候选药物,它们可能组合成一种潜在治疗慢性HBV感染方案。

乙肝研究药企,推进新药进展,上半年提供AB-729额外数据
Arbutus公司介绍,乙肝病毒可引起慢性感染,从而导致更高的肝硬化和肝癌死亡风险。慢性HBV感染是一种重要的尚未得到满足的医疗需求领域。尽管目前已有有效的疫苗和治疗方案,但每年仍有大约90万人死于与慢性HBV感染相关的并发症。AB-729,目前正在进行一项1a/1b期单剂量和多剂量临床试验,以确定AB-729在健康受试者和慢性HBV感染受试者中的安全性、耐受性、药代动力学和药效学。
迄今为止的结果表明,使用60毫克和90毫克剂量的AB-729单次治疗后,其对受试者耐受性良好。每4周重复给药60毫克剂量后,观察到第24周时,可以导致连续和稳健的平均乙肝表面抗原(HBsAg)水平下降(-1.84 log10 IU/mL, N=7)。每8周重复给药60毫克剂量后,所观察到结果可与——每4周重复给药60毫克剂量相比,它们在第16周时,平均乙肝表面抗原下降对照数据为-1.37 log10 IU/mL vs -1.44 log10 IU/mL, p
在HBVDNA阳性的慢性乙肝患者中,单个90毫克AB-729剂量,可导致强劲的平均乙肝表面抗原 (-1.02 log10 IU/mL)和HBVDNA (-1.53 log10 IU/mL)在第12周下降,以及HBVRNA和乙肝核心抗原水平下降。在HBVDNA阳性和阴性慢性乙肝受试者中,AB-729支持完全靶向的平均乙肝表面抗原减少。Arbutus公司预计,将于2021年上半年提供AB-729第1a/1b期临床试验队列额外数据,除了预计于2021年下半年提供的90毫克/12周队列的初始数据。
基于上述结果,Arbutus公司计划在2021年下半年,将AB-729推进到两个2期联合试验中,使用1种或者多种已批准或正在研究的药物,AB-729的给药频率为每8周或12周1次。目前,Arbutus公司还与Assembly公司,正在开展一项2期概念验证的联合临床试验,该试验将开始筛选AB-729与Assembly Biosciences公司的候选药物:乙肝病毒核心抑制剂vebicorvir(ABI-H0731)和1种核苷逆转录酶抑制剂(Nrtl),进行联合用于治疗慢性HBV感染受试者。
以上这项联合试验是一项随机、多中心、开放标签的2期临床试验,将评估vebicorvir(ABI-H0731)、AB-729和1种Nrtl的三联疗法的安全性、药代动力学和抗病毒活性,并与vebicorvir(ABI-H0731)和1种Nrtl、AB-729和1种Nrtl的双联疗法进行比较。预计大约有60名乙肝e抗原阴性的病毒学抑制的慢性HBV患者,将被纳入到本试验的第一队列。
受试者将给药48周,每日口服300毫克vebicorvir,每8周皮下注射60毫克AB-729,随访48周。Arbutus公司旗下另一种乙肝在研新药AB-836,这是一种口服衣壳抑制剂。2020年1月份,该公司选择AB-836作为下一代口服衣壳抑制剂。它属于一种新的化学系列,区别于具有提高疗效和增强抗性的潜在竞争化合物。Arbutus公司于2020年第四季度完成了CTA/IND支持研究,并计划于2021年上半年,启动AB-836的第1a/1b期临床试验。

上述两种研究药物AB-729和AB-836,目前均未上市,正处于临床试验中。Arbutus公司的药物研发侧重点,主要集中在其目前HBV新药研发管线的后续化合物和新的小分子抗病毒药物开发。
上一篇:全国人大代表徐镜人:加速提升中药新药创新能
下一篇:没有了